← Bewerbung Als Produktionshelfer Ohne Stellenangebot Muster Bewerbung Als Buchhalterin Muster Brandschutzordnung Teil B Vorlage Word →
Wenn das metall verformt wird werden die atomrümpfe und die elektronen lediglich verschoben.
Metallische bindung beispiel. Zwischen nichtmetallen und metallen wirken hingegen ionische und zwischen. Beryllium hingegen ist in der 2. Warum halten die metallatome eigentlich zusammen.
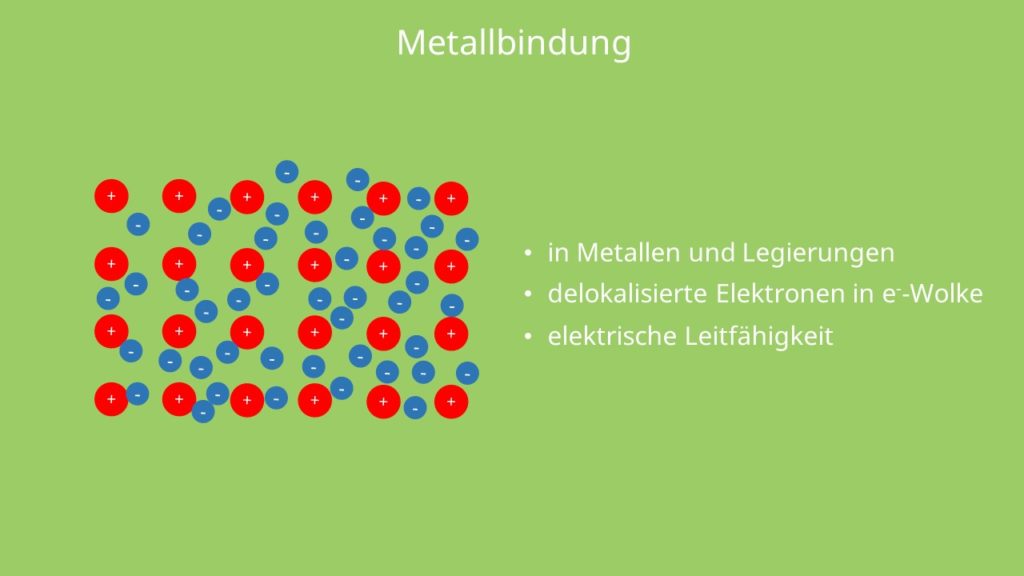
Kovalente und polare bindung liefern moleküle und werden mit molekülformeln beschrieben. Die atombindung auch kovalente bindung elektronenpaarbindung oder homöopolare bindung ist eine form der chemischen bindungen und ist als solche für den festen zusammenhalt von atomen in vielen chemischen verbindungen verantwortlich. Diese ist durch das auftreten von frei beweglichen delokalisierten elektronen im metallgitter gekennzeichnet die unter anderem für die makroskopischen eigenschaften elektrische leitfähigkeit metallischer glanz duktilität schmiedbarkeit verformbarkeit verantwortlich sind.
Die gute verformbarkeit der metalle ist ebenfalls eine folge der metallischen bindung. Die kovalente und die ionische bindung. Ionische und metallische bindung liefern gitter und werden mit verhältnisformeln beschrieben.
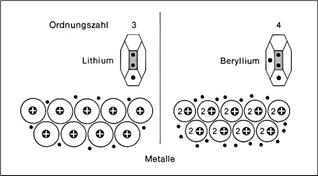
Wie du siehst befindet sich lithium in der 1. Wir haben das bisher im chemieunterricht zum beispiel beim atommodell kennengelernt und haben dort die drei modelle das volumenmodell das kern schale modell und das bohr modell unterschieden. Bei der chemischen bindung haben wir bisher zwei typen auf diese weise kennengelernt.
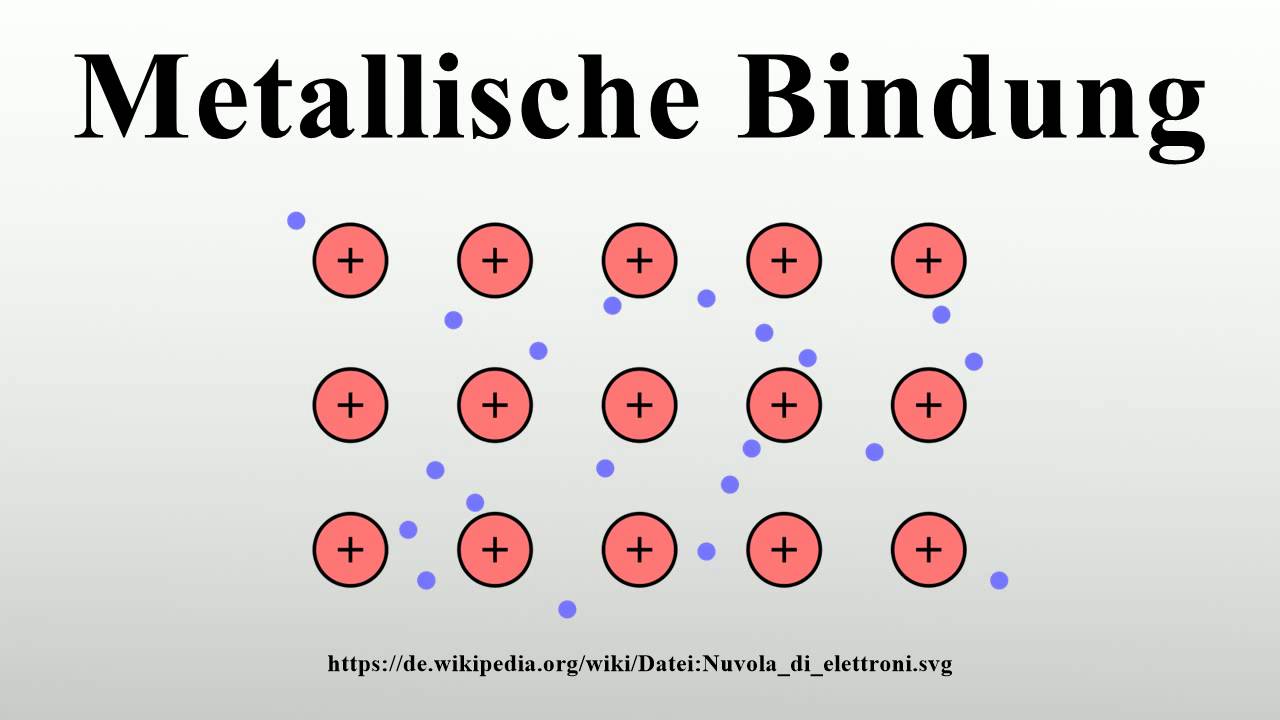
Zwischen verschieden geladenen ionen herrscht elektrostatische anziehung. Im prinzip ist jedes metallstück so es als festkörper vorliegt ein typisches beispiel für eine metallbindung. Die metallbindung wird durch die starke anziehung zwischen den positiv geladenen atomrümpfen und dem negativ geladenen elektronengas zusammengehalten.
Hauptgruppe und besitzt somit lediglich ein valenzelektron. Zwischen molekülen herrschen van der waals oder dipol kräfte. Um dir die metallbindung anhand ein paar beispiele genauer anzuschauen kannst du einen blick auf die linke seite im periodensystem werfen.
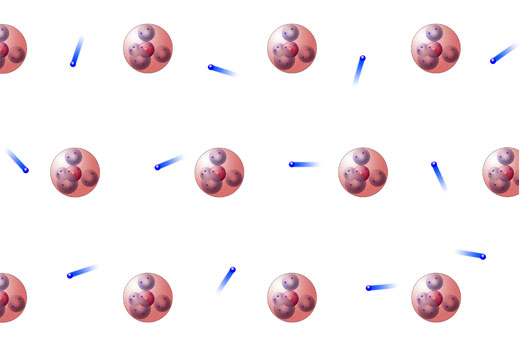
Werde einser schüler und klick hier https www thesimpleclub de gowie sind metalle gebunden. Die elektronen sind frei im metall beweglich. Atombindungen bilden sich besonders zwischen den atomen von nichtmetallen aus.
Die metallbindung ist eine art der chemischen bindung die durch anziehungskräfte zwischen metall ionen und freien elektronen verursacht wird. Legt man eine elektrische spannung von zum beispiel 6 volt gleichstrom an so fangen die elektronen an sich in eine bestimmte richtung zu bewegen nämlich in richtung auf den pluspol. Hauptgruppe und kann somit 2 valenzelektronen abgeben.
Am bekanntesten dürften jedoch eisen kupfer sowie aluminium sein.