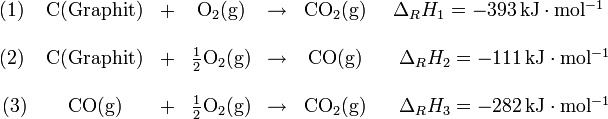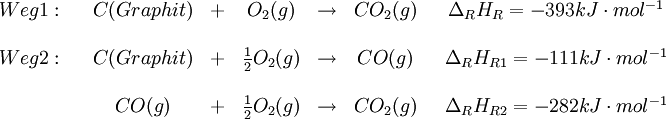← Schriftliches Referat Beispiel Schufa Auskunft Beispiel Schön Schreiben Lernen Vorlagen →
Unter dem abzug gearbeitet werden.
Satz von hess beispiel. Zunächst noch ein weiteres beispiel nach dem weg von atkins. Satz von hess hess scher wärmesatz. Dies wird als der satz von hess bezeichnet.
Standarbildungsenthalpien von methan. Der hess sche wärmesatz auch satz von hess dient der berechnung von enthalpie änderungen bei chemischen reaktionen er wurde 1840 von germain henri hess aufgestellt. Der energieumsatz bei der bildung von glucose aus kohlendioxid und wasser ist genau so groß wie der umsatz bei der verbrennung von glucose nur das vorzeichen ändert sich.
In diesem video zeige ich dir anhand eines beispiels die anwendung des satzes von hess. Der satz von heß heßscher wärmesatz besagt daß die reaktionsenthalpie nur vom zustand der edukte und produkte abhängt nicht vom reaktionsverlauf und der anzahl der schritte. Der reaktionsweg hat dabei nach dem energieerhaltungssatz keinen einfluss auf die energie die bei einer reaktion aufgenommen.
Bildung von kohlenstoffdioxid aus den elementen kohlenstoffdioxid kann durch direkte verbrennung von kohlenstoff an luft hergestellt werden weg a. In vielen fällen können produkte einer chemischen reaktion auf verschiedenen wegen entstehen. Satz von hess am beispiel des lösens und neutralisierens von naoh lit.
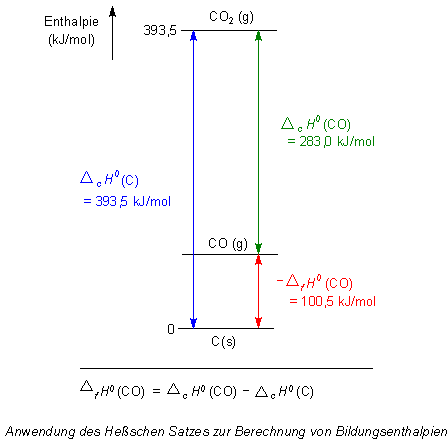
Endotherme reaktionen mit starker entropie zunahme siehe lösungsenthalpie kno3 ba oh 2 8h2o 2 nh4scn 2 nh3 ba scn 2 10 h2o verdunsten von. Es sollte deshalb ggf. Durch anwendung des satzes von heß können reaktionsenthalpien indirekt bestimmt werden die experimentell nicht direkt gemessen werden können beispielsweise die bildungsenthalpie von kohlenmonoxid co.
Heßscher satz ältere bezeichnung gesetz der konstanten wärmesummen eine spezielle anwendung des 1. V 3 versuch zum wärmesatz von hess bei der reaktion von calcium mit salzsäure 5 bei diesem versuch ist darauf zu achten dass durch den wasserstoff keine gefahr entsteht. Der reaktionsweg hat dabei nach dem energieerhaltungssatz keinen einfluss auf die energie die bei einer reaktion aufgenommen oder.
Es besteht aber auch die möglichkeit dass bei der verbrennung zunächst erst nur kohlenstoffmonooxid entsteht weg b1 dass dann in einem. Der hess sche wärmesatz auch satz von hess dient der berechnung von enthalpieänderungen bei chemischen reaktionen er wurde 1840 von germain henri hess aufgestellt. Chemie heute sek ii s 62 4 g naoh 100 ml h2o 50 ml naoh 50 ml hcl c 2 mol l 4 g naoh 100 ml hcl c 1 mol l v.
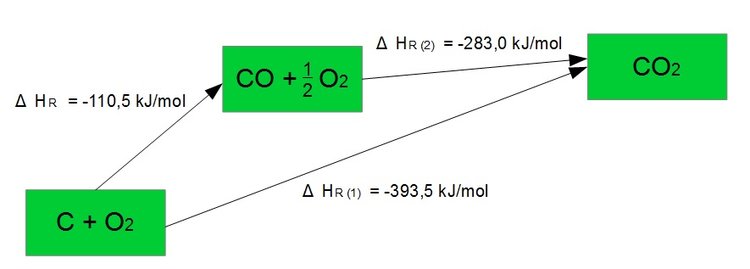
Im anschluss werden auch überlegungen aufgezeigt wie man den satz von hess noch anwenden kann. Dabei ist bei verschiedenen reaktionswegen mit den gleichen ausgangs und endstoffen die summe der reaktionswärmen auf jedem dieser wege gleich.