← Pflegeplanung Vorlage Word Muster Widerrufsbelehrung 2002 Photoshop Muster Erstellen →
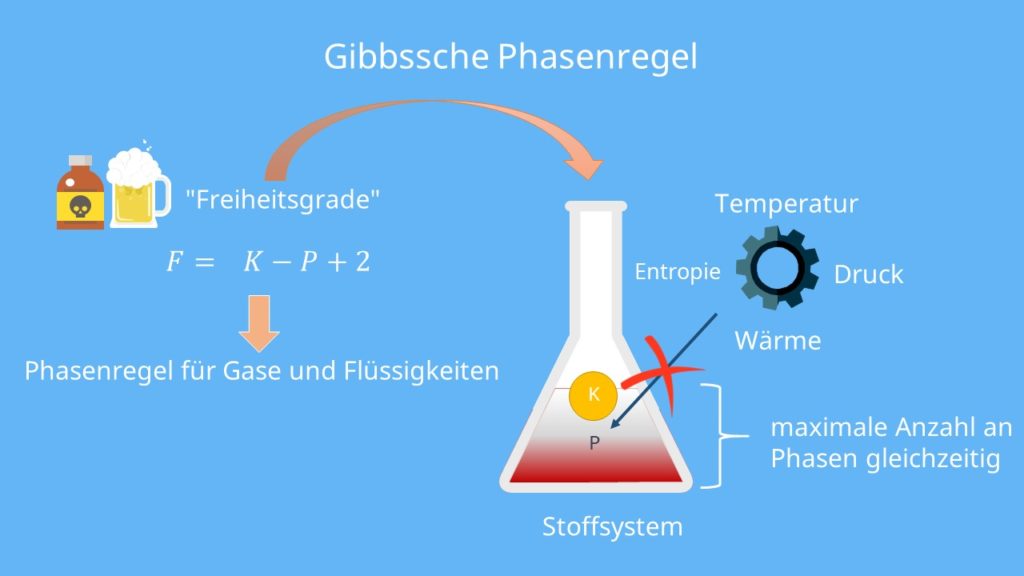
Zudem kann man mit ihr die an einem bestimmten punkt im phasendiagramm maximal möglichen freiheitsgrade bestimmen.
Gibbssche phasenregel beispiel. Für ein physikalisch homogenes thermodynamisches system reichen zwei zustandsgrößen zur bestimmung des gleichgewichtszustands. Eingesetzt in die gibbs sche phasenregel ergibt sich die anzahl der zustandsgrößen die für die diamantenherstellung berücksichtigt werden müssen. Gibbssche phasenregel gibbssches phasengesetz thermodynamisch abzuleitender und durch die erfahrung bestätigter zusammenhang zwischen der anzahl p der phasen in einem sich im thermodynamischen gleichgewicht befindenden heterogenen system aus k komponenten und der anzahl f der thermodynamischen freiheitsgrade.
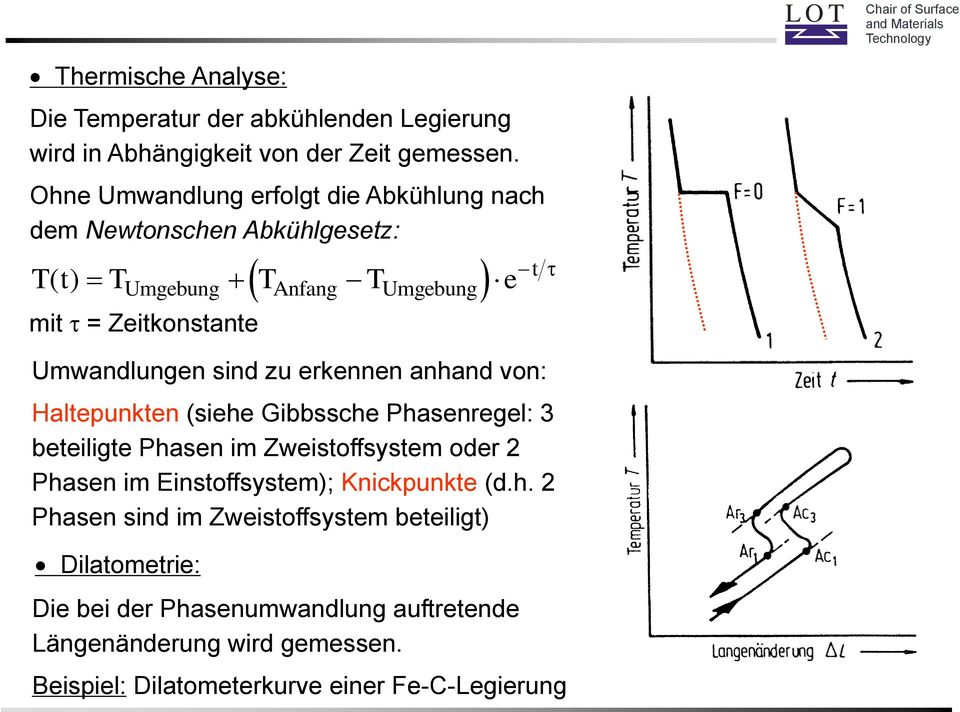
Beispielsweise liegt der tripelpunkt von kohlenstoffdioxid genau bei 216 55k was entspricht und 5180hpa. Die gibbssche phasenregel nach josiah willard gibbs 1876 beinhaltet die aussage dass im thermodynamischen gleichgewicht nicht beliebig viele phasen gleichzeitig nebeneinander vorliegen können. F k p 2 1 1 2 2.
Diamanten bestehen aus kohlenstoff k 1 in fester form p 1. Für ein physikalisch homogenes thermodynamisches system reichen zwei. Somit ergibt sich die gibbssche phasenregel als.
Zudem kann man mit ihr die an einem bestimmten punkt im phasendiagramm maximal möglichen freiheitsgrade bestimmen. Die gibbssche phasenregel nach josiah willard gibbs 1876 auch einfach phasengesetz gibt an wie viele freiheitsgrade ein im thermodynamischen gleichgewicht befindliches system in abhängigkeit von der zahl der enthaltenen substanzen und der zahl der gleichzeitig existierenden phasen besitzt. Zudem kann man mit ihr die an einem bestimmten punkt im phasendiagramm maximal möglichen freiheitsgrade bestimmen.
Anwendung der gibbs schen phasenregel. Die gibbssche phasenregel nach josiah willard gibbs 1876 auch einfach phasengesetz hält fest dass im thermodynamischen gleichgewicht nicht beliebig viele phasen gleichzeitig nebeneinander vorliegen können. Für ein physikalisch homogenes.